目前,國內取得藥品監督管理部門(mén)批準產(chǎn)品注冊證的醫療器械生產(chǎn)企業(yè)有2000多家,外國采購商可選擇的供貨商數量充足,供貨質(zhì)量有保障。截至4月4日,已有54個(gè)國家和地區以及3個(gè)國際組織和中國企業(yè)簽署了醫療物資商業(yè)采購合同。
為做好新冠肺炎疫情防控和經(jīng)濟社會(huì )發(fā)展工作,支持企業(yè)復工復產(chǎn),針對企業(yè)不熟悉防疫物資出口政策等實(shí)際問(wèn)題,4月4日,中國國家認證認可監督管理委員會(huì )就口罩等防疫用品出口歐盟及美國的相關(guān)準入要求及梳理的國內具有相應資質(zhì)能力的認證機構名錄提供信息指南,供企業(yè)參考。
一、歐盟對口罩等防疫用品準入要求
(一)口罩
歐盟根據用途將口罩分為兩類(lèi):醫用口罩和個(gè)人防護口罩。
1.醫用口罩
醫用口罩需按照歐盟醫療器械指令93/42/EEC(MDD)或歐盟醫療器械條例EU2017/745(MDR)加貼CE標志,對應的標準是EN14683。根據口罩產(chǎn)品無(wú)菌或非無(wú)菌狀態(tài),采取的合格評定模式也不同。(1)無(wú)菌醫用口罩:必須由授權公告機構進(jìn)行CE認證。
(2)非無(wú)菌醫用口罩:企業(yè)只需進(jìn)行CE自我符合性聲明,不需要通過(guò)公告機構認證。在準備好相應文件及測試報告等資料后,即可自行完成符合性聲明。
2.個(gè)人防護口罩
個(gè)人防護口罩不屬于醫療器械,但需符合歐盟個(gè)人防護設備條例EU2016/425(PPE)要求,由授權公告機構進(jìn)行CE認證并頒發(fā)證書(shū),對應的標準是EN149。
(二)防護服
防護服也分為醫用防護服和個(gè)人防護服,管理要求與口罩基本類(lèi)似。醫用防護服按照醫療器械管理,其中無(wú)菌醫用防護服需按照歐盟醫療器械指令93/42/EEC(MDD)或歐盟醫療器械條例EU2017/745(MDR)獲得CE認證,非無(wú)菌醫用防護服只需進(jìn)行CE自我聲明。個(gè)人防護服需按照歐盟個(gè)人防護設備條例EU2016/425(PPE)獲得CE認證。
(三)歐盟公告機構查詢(xún)地址
1.歐盟醫療器械指令93/42/EEC(MDD)授權的公告機構查詢(xún)地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13
2.歐盟醫療器械條例EU 2017/745(MDR)授權的公告機構查詢(xún)地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34
3.歐盟個(gè)人防護裝備條例EU2016/425(PPE)授權的公告機構查詢(xún)地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=155501
二、美國對口罩等防疫用品準入要求
(一)口罩
美國對醫用口罩和防護口罩同樣區分管理,其中醫用口罩由美國食品藥品監督管理局(FDA)管理,而個(gè)人防護口罩則由美國國家職業(yè)安全衛生研究所(NIOSH)管理。
1.醫用口罩
醫用口罩需通過(guò)FDA注冊,企業(yè)直接向FDA官網(wǎng)申請并提交相關(guān)材料。此外還有兩種可選途徑:
(1)已經(jīng)獲得NIOSH注冊的N95口罩,在產(chǎn)品生物學(xué)測試、阻燃測試和血液穿透測試通過(guò)的情況下,可以豁免產(chǎn)品上市登記(510K),直接進(jìn)行FDA工廠(chǎng)注冊和醫療器械列名。
(2)如果獲得持有510K的制造商的授權,可以作為其代工廠(chǎng)使用其510K批準號進(jìn)行企業(yè)注冊和器械列名。
2.個(gè)人防護口罩
防護口罩需通過(guò)NIOSH注冊,企業(yè)直接在NIOSH官網(wǎng)申請。
(二)防護服
對醫用防護服和個(gè)人防護服的管理也類(lèi)似于口罩的管理方式,其中醫用防護服由美國食品藥品監督管理局(FDA)管理,而個(gè)人防護服由美國國家職業(yè)安全衛生研究所(NIOSH)管理。企業(yè)直接在FDA或NIOSH進(jìn)行注冊申請。
三、中國境內具有口罩等防疫用品CE認證能力的認證機構名錄
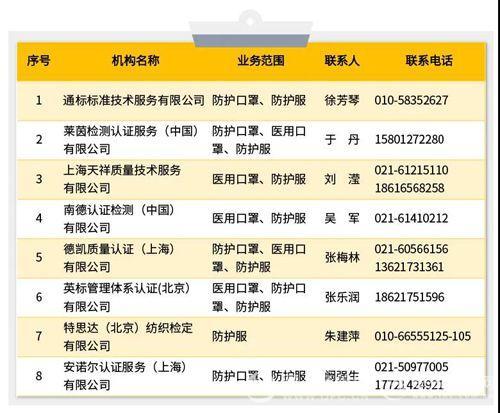
四、中國境內可以開(kāi)展醫療器械管理體系(ISO13485)認證的機構名錄
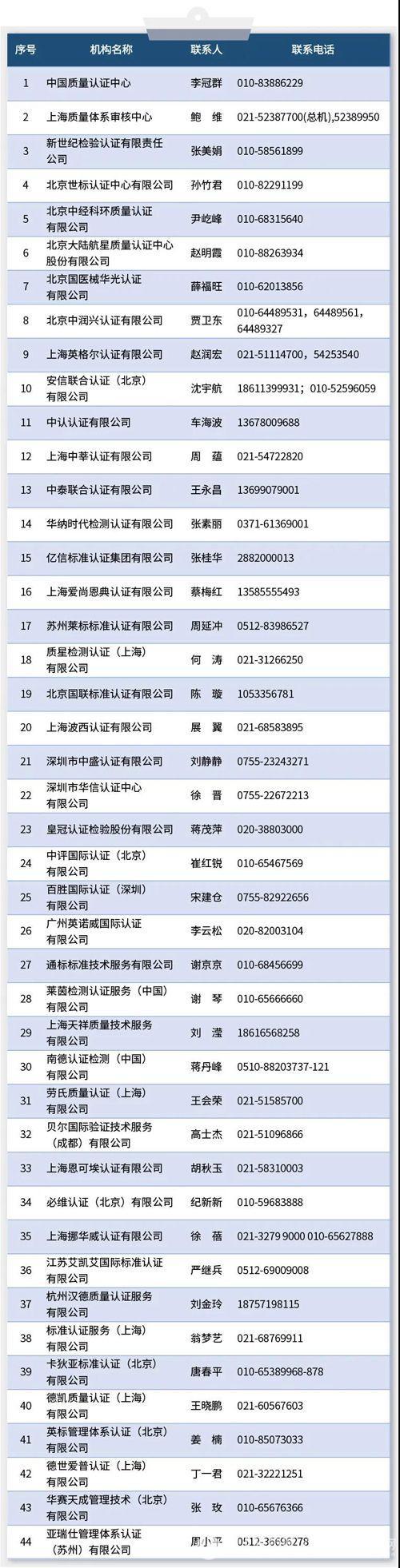
(來(lái)源:中國紡織報)
來(lái)源: 中國紡織工業(yè)聯(lián)合會(huì )
相關(guān)資訊
- 打贏(yíng)“生存戰”,看日本紡企如何上演合縱連橫
- 波蘭之旅,開(kāi)啟中波紡織服裝合作新篇章
- BRICS+金磚國家時(shí)尚峰會(huì )加強全球時(shí)尚聯(lián)系
- 《2023紡織業(yè)對外投資合作國別指南》拉美篇(一)——墨西哥
- 國際紡織機械展覽會(huì )孟加拉國觀(guān)眾組織推介會(huì )再獲關(guān)注
- 三分鐘導讀紡織行業(yè)宏觀(guān)經(jīng)濟環(huán)境
- 衣心向善!中法可持續時(shí)尚行業(yè)分享綠色轉型經(jīng)驗及案例
- 上半年全國紡織品服裝出口同比下降,RCEP機遇值得重點(diǎn)關(guān)注
- 上半年全國紡織品服裝出口同比下降,RCEP機遇值得重點(diǎn)關(guān)注
- 2022世界變局下的日本紡企應對之策(下)
- 堅持開(kāi)放包容、創(chuàng )新發(fā)展、合作共贏(yíng),國際紡聯(lián)紡機研討會(huì )發(fā)出業(yè)界最強音
- 2022世界變局下的日本紡企應對之策(下)
更多推薦供應
更多求購信息
更多加工信息
- 承接各種男女裝童裝毛衣加工業(yè)務(wù)
- 生產(chǎn)銷(xiāo)售印紙印花 花型花紙及加工
- 峰德針織內衣承接內衣產(chǎn)品加工銷(xiāo)售業(yè)務(wù)
- 吳中郭巷創(chuàng )威激光加工激光切割機打標
- 承接男裝、休閑服裝等產(chǎn)品生產(chǎn)加工業(yè)務(wù)
- 浙銘沖孔制品廠(chǎng)承接沖孔、切雕加工業(yè)務(wù)
- 承接內外貿毛衣生產(chǎn)毛衣貼牌加工
- 松崗戴琦詩(shī)服裝廠(chǎng)承接服裝加工業(yè)務(wù)
- 承接男式T恤衫,POLO衫加工銷(xiāo)售業(yè)務(wù)
- 承接戶(hù)外服裝、沖鋒衣軟殼沖鋒衣加工
資訊排行
- 起舞·織夢(mèng)未來(lái) | 數據看紡織,從限量供應到位居世界之首
- 時(shí)尚產(chǎn)業(yè)流通轉型升級路怎么走?無(wú)錫這場(chǎng)圓桌會(huì )議帶來(lái)實(shí)用指南
- “AI+紡織”在行動(dòng)|智能革新:AI 重塑紡織服裝行業(yè)的未來(lái)
- 纖維之路×恒田企業(yè)×亞?wèn)|集團×天虹紡織|2024中國纖維流行趨勢對接交流活動(dòng)走進(jìn)江蘇
- 2025濰坊(諸城)紡織服裝產(chǎn)業(yè)國際精準采購節即將啟幕
- 智慧賦能!打造“新智+新質(zhì)”產(chǎn)業(yè)電商新生態(tài)-紡織服裝周刊
- 新華社刊發(fā):“老”紡織“新”力量
- 中國紡聯(lián)啟動(dòng)《紡織服裝行業(yè)碳足跡管理體系》標準編制工作
- 鴻天集團核心業(yè)務(wù)持續增長(cháng),創(chuàng )新驅動(dòng)發(fā)展新篇章
- 花禧樂(lè )紡織:乘國風(fēng)之勢而起,舞動(dòng)時(shí)尚新姿
- 中國紡聯(lián)會(huì )長(cháng)孫瑞哲:堅定信心,干在實(shí)處,啟錦繡新篇,繪美好未來(lái)-紡織服裝周刊
- 中國紡聯(lián)會(huì )長(cháng)孫瑞哲:立高遠之意,行篤實(shí)之效,創(chuàng )開(kāi)闊之境!
- 第八屆中國紡織非遺大會(huì )將于11月在海寧許村舉辦
- 山東聯(lián)潤新材料科技有限公司董事長(cháng)兼總經(jīng)理陳啟升:為美好生活創(chuàng )新
- “烏蒙村秀”新年唱響彝族服飾時(shí)尚新樂(lè )章
視覺(jué)焦點(diǎn)
-
 35個(gè)!2024年國家先進(jìn)制造業(yè)集群名單公布
35個(gè)!2024年國家先進(jìn)制造業(yè)集群名單公布
-
 產(chǎn)學(xué)研用 校企合作 助推產(chǎn)業(yè)設計創(chuàng )新升級
產(chǎn)學(xué)研用 校企合作 助推產(chǎn)業(yè)設計創(chuàng )新升級
-
 2024中國紡織服裝行業(yè)年度大盤(pán)點(diǎn)——十大新聞事件-紡織服裝周刊
2024中國紡織服裝行業(yè)年度大盤(pán)點(diǎn)——十大新聞事件-紡織服裝周刊
-
 武漢時(shí)裝周之今日非遺,變化中的新生
武漢時(shí)裝周之今日非遺,變化中的新生
-
 面臨新的機遇和挑戰 紡織行業(yè)鍛造競爭新優(yōu)勢
面臨新的機遇和挑戰 紡織行業(yè)鍛造競爭新優(yōu)勢
-
 世界布商大會(huì )
世界布商大會(huì )
-
 中國紡聯(lián)啟動(dòng)《紡織服裝行業(yè)碳足跡管理體系》標準編制工作
中國紡聯(lián)啟動(dòng)《紡織服裝行業(yè)碳足跡管理體系》標準編制工作
-
 2025濰坊(諸城)紡織服裝產(chǎn)業(yè)國際精準采購節即將啟幕
2025濰坊(諸城)紡織服裝產(chǎn)業(yè)國際精準采購節即將啟幕
-
 崛起之路|新賽道的領(lǐng)航者——記吉林工程技術(shù)師范學(xué)院教授張躍
崛起之路|新賽道的領(lǐng)航者——記吉林工程技術(shù)師范學(xué)院教授張躍
-
 質(zhì)領(lǐng)2025企業(yè)談|新鄉化纖黨委書(shū)記、董事長(cháng)邵長(cháng)金:向“新”求“質(zhì)”,逐夢(mèng)白鷺新篇-紡織服裝周刊
質(zhì)領(lǐng)2025企業(yè)談|新鄉化纖黨委書(shū)記、董事長(cháng)邵長(cháng)金:向“新”求“質(zhì)”,逐夢(mèng)白鷺新篇-紡織服裝周刊






